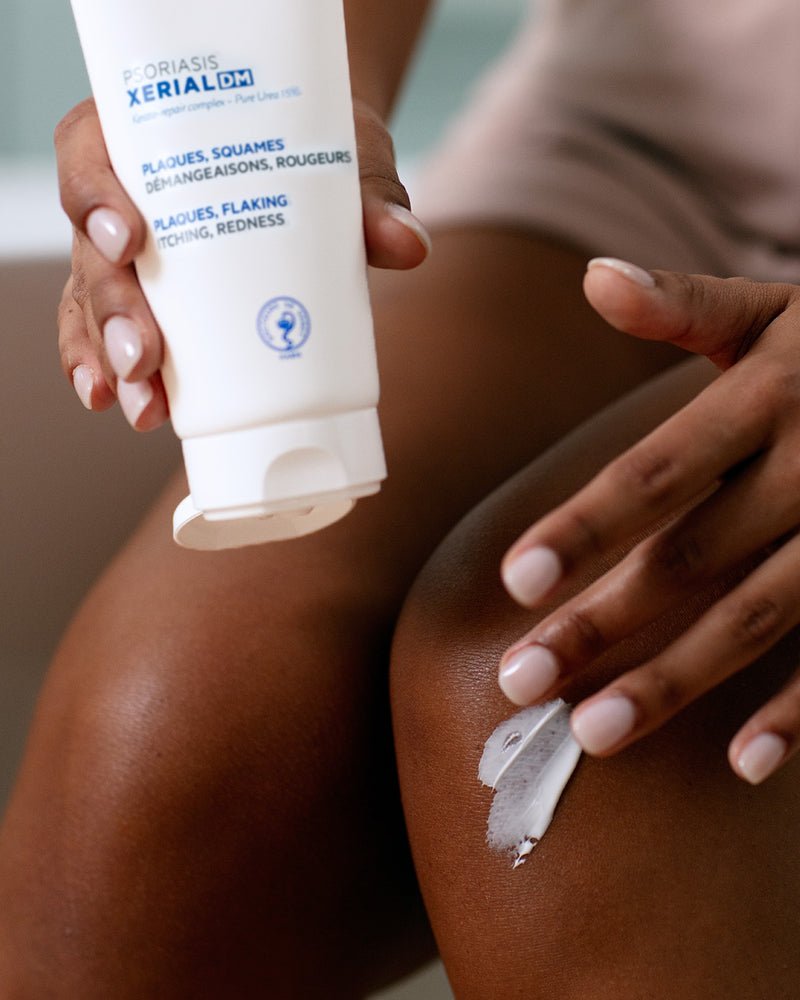



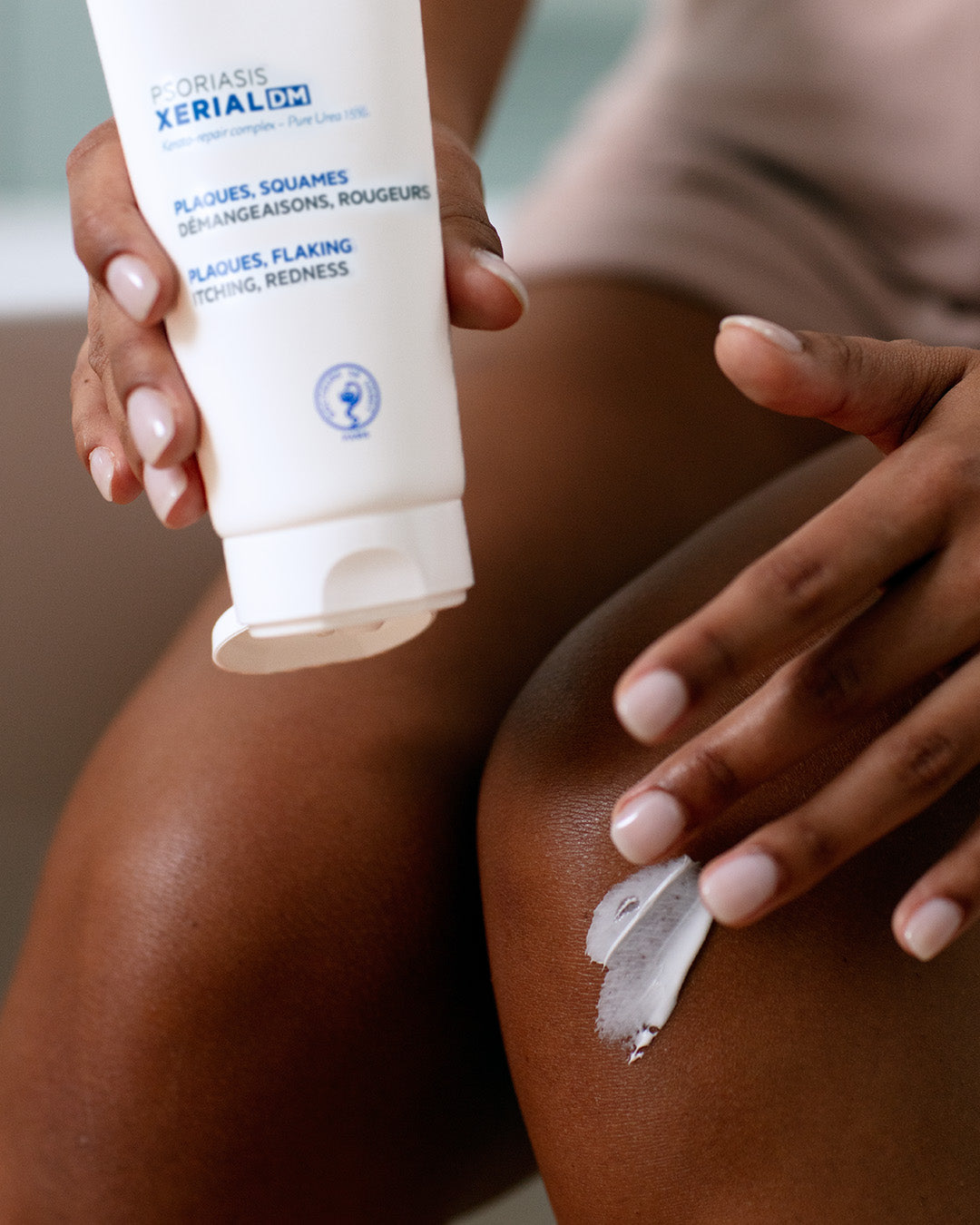


RÉSULTATS PROUVÉS
DES 14 JOURS
-27% des squames (1)
APRES 30 JOURS
-23% de rougeurs (1)
+19%
Amélioration de la plaque (PSI score total) (1)
96%
Des patients ont trouvé que sa texture filmogène était facile à appliquer (2)
(1) Investigation clinique multicentrique (centre 1 inactif), randomisée, en double aveugle et contrôlée par placebo sur 30 patients ayant 2 plaques de psoriasis (≈ 20 cm², espacé d’au moins 15cm), en deux phases séparées avec application de XERIAL DM Psoriasis ou placebo deux fois par jour sur les plaques de psoriasis pendant 30 jours pour la phase 1 et pendant 28 jours pour la phase 2 séparé par un traitement à base de calcipotriol et de bétamétasone (un dermocorticoïde). Rapport d’évaluation clinique du 09/11/2021 n° 03-DM-2018 – n° ID-RCB 2018-A03297-48. Evaluation du PSI score total et des sous-score desquamation et rugosité à 14 et 30 jours (phase 1) : PSI : n=30, moyenne (J0) = 7,50±1,22, moyenne (J14)=6,10±1,75 (p <0.001) ; diff. significative vs placebo ; Desquamation n=30, moyenne (J0) = 2,57±0,61, moyenne (J14) : 1,87±0,90 (p <0.001), diff. significative vs placebo ; Rougeurs n=30, moyenne (J0) = 2,60±0,50, moyenne (J30) : 2,00±0,79 (p <0.001), diff. significative vs placebo. Résultats de tolérance : 42,4 % des patients ont présenté un total de 24 effets indésirables d’intensité légère à modérée dont 13 possiblement liés aux produits de l’étude : 9 liés à XERIAL DM PSORIASIS et 4 au PLACEBO. Ces effets sont les suivants : picotements (9%), prurit (15%) et sensation de brûlure (3%). Tous les EIs liés étaient locaux et ont été résolus avant la fin de l’étude.
(2) Investigation clinique multicentrique (centre 1 inactif), randomisée, en double aveugle et contrôlée par placebo sur 30 patients ayant 2 plaques de psoriasis (≈ 20 cm², espacé d’au moins 15cm), en deux phases séparées avec application de XERIAL DM Psoriasis ou placebo deux fois par jour sur les plaques de psoriasis pendant 30 jours pour la phase 1 et pendant 28 jours pour la phase 2 séparé par un traitement à base de calcipotriol et de bétamétasone (un dermocorticoïde). Rapport d’évaluation clinique du 09/11/2021 n° 03-DM-2018 – n° ID-RCB 2018-A03297-48 . Autoévaluation à 7 jours (phase 2).
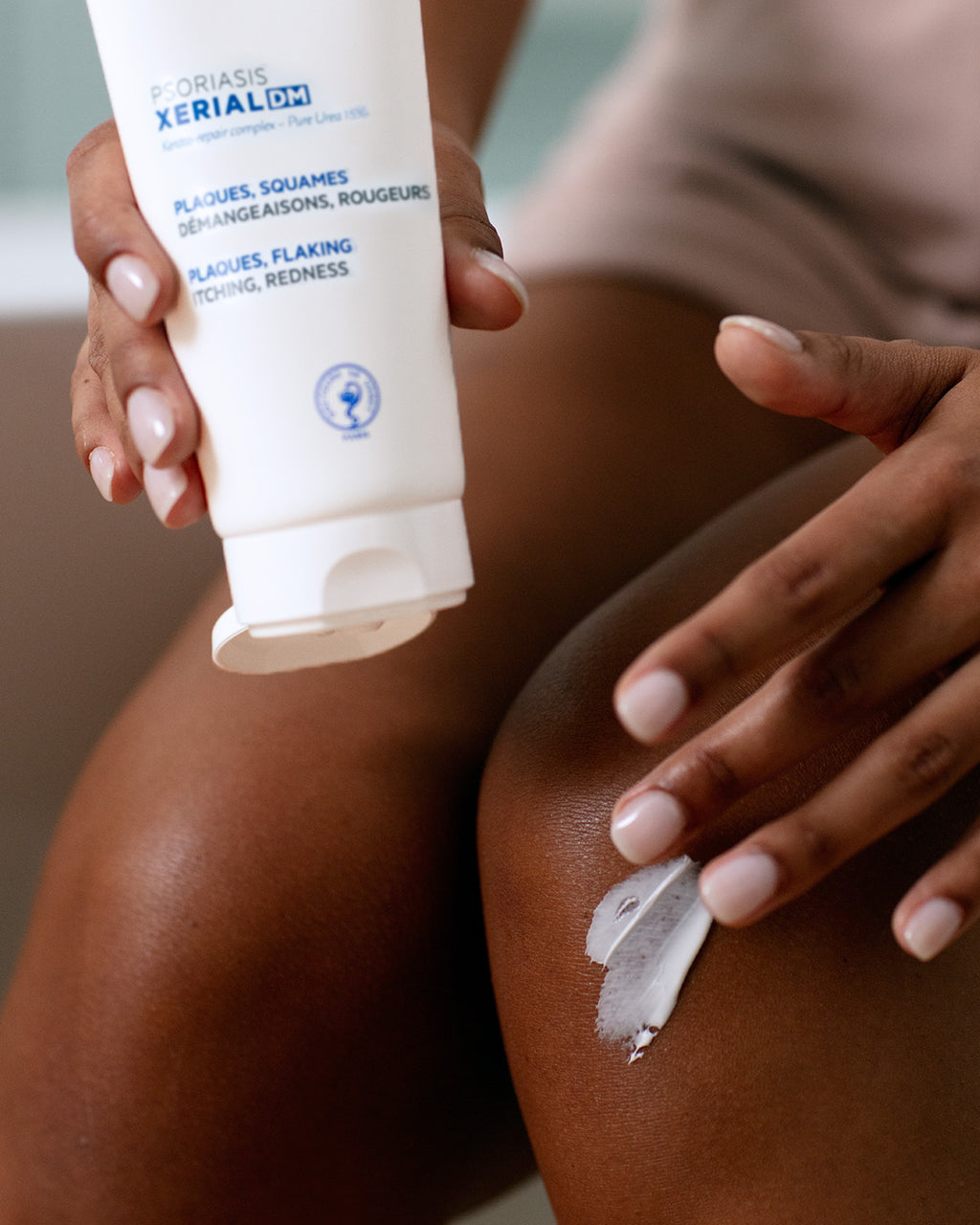
INGRÉDIENTS
COMPLEXE KERATO-REPARATEUR 15% D’URÉE PURE
Action kératolytique qui traite les plaques épaisses et réduit les squames. L’exopolysaccharide marin est issu d’une algue rouge bretonne, actif reconnu favorisant la réduction de la desquamation et hydrate la peau*. *Mammone, T.; Gan, D.; Fthenakis, C.; Marenus, K. The Effect of N-Acetyl-Glucosamine on Stratum Corneum Desquamation and Water Content in Human Skin. J. Cosmet. Sci. 2009, 60, 423–428.
AGENTS EMOLLIENTS 27%
Beurre de karité et huile de caméline : soulagent et protègent la peau
ORBIGNYA OLEIFERA SEED OIL, CAPRYLIC/CAPRIC TRIGLYCERIDE, DIMETHICONE, GLYCERIN, PROPANEDIOL, GLYCOL PALMITATE, GLYCERYL STEARATE, PEG-100 STEARATE, MYRISTYL ALCOHOL, CAMELINA SATIVA SEED OIL, HYDROXYETHYL ACRYLATE/SODIUM ACRYLOYLDIMETHYL TAURATE COPOLYMER, CERA ALBA/BEESWAX/CIRE D'ABEILLE, SODIUM CITRATE, TRIACETIN, MYRISTYL GLUCOSIDE, PENTYLENE GLYCOL, POLYACRYLATE CROSSPOLYMER-6, DIMETHICONE CROSSPOLYMER, CITRIC ACID, TOCOPHEROL, 1,2-HEXANEDIOL, CAPRYLYL GLYCOL, PARFUM (FRAGRANCE), CALCIUM PCA, SODIUM LACTATE, GLYCINE SOJA (SOYBEAN) OIL, STEARYL STEARATE, STEARYL PALMITATE, HYDROLYZED HYALURONIC ACID, PARAFFIN, POLYSORBATE 60, SORBITAN ISOSTEARATE, CETYL PALMITATE, CETYL STEARATE, SACCHARIDE ISOMERATE, BEHENIC ACID, STEARIC ACID, CERA MICROCRISTALLINA/MICROCRYSTALLINE WAX/CIRE MICROCRISTALLINE, ARACHIDIC ACID, PALMITIC ACID, HELIANTHUS ANNUUS (SUNFLOWER) SEED OIL









![LA GAMME [A] [B<sub>3</sub>] [C]](http://ma.svr.com/cdn/shop/collections/Megaroll_3000x2000_desktop_abc_1800x_e9f12695-29db-4b75-b668-8a5d4eeed1f0.jpg?crop=center&height=750&v=1684324684&width=500)